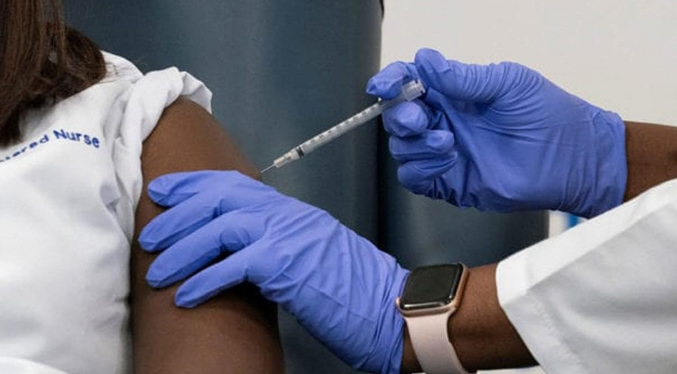
Un panel médico que asesora al gobierno de Estados Unidos votó el viernes a favor de un refuerzo de la vacuna Pfizer contra el covid a los mayores de 65 años y a aquellos con alto riesgo de desarrollar covid grave, pero rechazó una tercera dosis para los mayores de 16.
Los expertos recomendaron que esta dosis de refuerzo se administre a partir de los seis meses de la segunda dosis.
La aprobación se celebró en una segunda votación tras haber rechazado previamente, con amplio respaldo, el plan de una tercera dosis para la mayoría de la población, al considerar insuficientes las pruebas para administrar una tercera dosis a todo el mundo.
De este modo se restringe la petición de Pfizer, que había solicitado la aprobación para las personas mayores de 16 años de este refuerzo, seis meses después de la segunda dosis.
En particular, mencionaron preocupaciones sobre los riesgos de miocarditis, una inflamación del músculo cardíaco, en varones adolescentes jóvenes y varones adultos.
“Creo que esto debería demostrarle al público en general que los miembros de este comité son independientes de la FDA, y que tenemos algo que decir cuando se nos invita a sentarnos”, dijo uno de sus miembros, Archana Chatterjee.
Critican la prisa de Biden
El doctor Paul Offit criticó el apresuramiento mostrado por el Gobierno del presidente estadounidense, Joe Biden, y la farmacéutica para lograr esta autorización general.
“Esta es una gran decisión (…) No entiendo cuál es la razón por la que no podamos dedicar más tiempo a mirar los datos”, indicó Offit, del Centro de Educación de Vacunas del Hospital Infantil de Filadelfia (Pensilvania) durante el debate.
Por su parte, Michael Kurilla, especialista en enfermedades infecciosas de los Institutos Nacionales de la Salud (NIH, en inglés) de EEUU remarcó que “no está claro que todo el mundo necesite el refuerzo, más allá del pequeño grupo de población que claramente estaría en alto riesgo de una enfermedad grave”.
La votación del panel de asesores de la FDA no es vinculante pero suele ser respetada por la agencia a la hora de emitir sus decisiones.
La recomendación supone un toque de atención para el Gobierno de Biden, que había dado su apoyo explícito a la propuesta y comenzado a hacer planes para iniciar la administración de esta tercera dosis a los mayores de 16 años con la vista puesta en el 20 de septiembre.
Entre los argumentos de apoyo al refuerzo los expertos de Pfizer citaron el repunte de casos por la variante delta, especialmente contagiosa, y las pruebas crecientes de que la protección de la vacuna comienza a disminuir con el tiempo.
Por Agencia