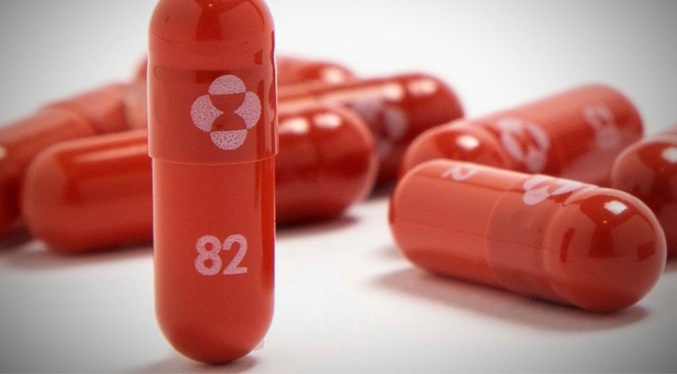
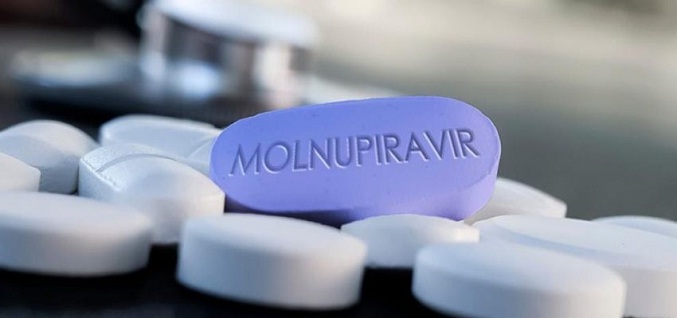
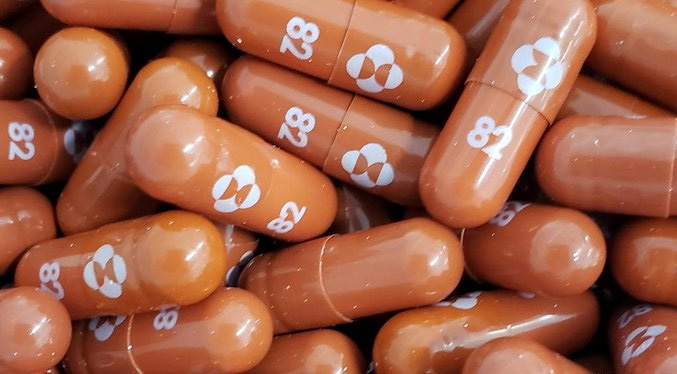
Estados Unidos autoriza la pastilla de Merck contra el COVID-19
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) anunció este jueves (23.12.2021) que autoriza el uso de la pastilla anticovid del laboratorio Merck para adultos de alto riesgo, un día después de que diera luz verde a una similar de Pfizer. El tratamiento se debe aplicar a personas con síntomas leves o moderados y que tengan mayores riesgos de ser hospitalizados o morir debido a su edad o enfermedades previas, incluyendo asma y obesidad.
"La autorización de hoy proporciona una opción de tratamiento adicional contra el virus SARS-CoV-2 en forma de pastilla que se puede tomar por vía oral", dijo Patrizia Cavazzoni, científica de la FDA, entidad que advirtió por medio de un comunicado que este tratamiento solo debe usarse cuando no haya otro mejor disponible.
La pas...